界面新聞記者 | 唐卓雅
界面新聞編輯 | 謝欣
信達(dá)生物的雙靶點(diǎn)減肥藥瑪仕度肽研發(fā)又有新進(jìn)展。
1月9日早間,信達(dá)生物官微發(fā)布文章稱,胰高血糖素樣肽-1受體(GLP-1R)/胰高血糖素受體(GCGR)雙重激動劑瑪仕度肽在中國超重或肥胖成人受試者中的首個III期臨床研究(GLORY-1)達(dá)成主要終點(diǎn)和所有關(guān)鍵次要終點(diǎn)。
也就是說,這款雙靶點(diǎn)減肥藥的三期臨床試驗獲得成功。
并且,信達(dá)生物稱,計劃近期向國家藥品監(jiān)督管理局(NMPA)藥品審評中心(CDE)遞交瑪仕度肽減重適應(yīng)癥的首個新藥上市申請(NDA)。目前,瑪仕度肽是國內(nèi)研發(fā)進(jìn)度最快的雙靶點(diǎn)創(chuàng)新藥。如果上市成功,瑪仕度肽將成為首個國產(chǎn)減重GCGR/GLP-1R雙靶點(diǎn)創(chuàng)新藥。
1月9日,信達(dá)生物股價開盤高漲5.61%,截至收盤漲1.96%,報39.05元/股。而今年開年以來,信達(dá)生物股價總體一路走低,1月2日至1月8日跌去了10.41%。

瑪仕度肽是信達(dá)生物與禮來制藥共同推進(jìn)的一款GLP-1R/GCGR雙重激動劑。2019年8月,信達(dá)生物和禮來達(dá)成合作,在中國共同開發(fā)和商業(yè)化這款候選藥物。也就是說,信達(dá)生物僅有瑪仕度肽在國內(nèi)的商業(yè)化權(quán)益。
目前,瑪仕度肽在中國超重或肥胖(GLORY-1和GLORY-2)受試者和2型糖尿病(DREAMS-1和DREAMS-2)受試者中的四項III期注冊研究正在進(jìn)行中。此外,2023年12月26日,信達(dá)生物啟動了瑪仕度肽頭對頭司美格魯肽的III期臨床試驗,研究的人群為早期2型糖尿病合并肥胖患者。 其中,GLORY-1研究已經(jīng)達(dá)成主要終點(diǎn)和所有關(guān)鍵次要終點(diǎn)。
具體來看,GLORY-1(NCT05607680)是一項在超重或肥胖受試者中評估瑪仕度肽的有效性和安全性的多中心、隨機(jī)、雙盲、安慰劑對照的III期臨床研究。研究入組610例受試者,隨機(jī)分配至瑪仕度肽4mg組、瑪仕度肽6mg組或安慰劑組,雙盲治療48周。
研究結(jié)果顯示,GLORY-1的兩個主要研究終點(diǎn)均順利達(dá)成:瑪仕度肽4mg和6mg組受試者治療32周后體重相對基線的百分比變化,以及體重相對基線下降≥5%的受試者比例均顯著優(yōu)于安慰劑組;第48周時,瑪仕度肽組的減重療效較32周進(jìn)一步提升。
此外,該研究所有關(guān)鍵次要終點(diǎn)均順利達(dá)成,與安慰劑相比,瑪仕度肽組體重相對基線下降≥10%和≥15%的受試者比例、以及腰圍等指標(biāo)的改善均顯著優(yōu)于安慰劑。
信達(dá)生物稱,雙盲治療期內(nèi),瑪仕度肽整體安全性良好,安全性特征與瑪仕度肽的既往臨床研究一致,未發(fā)現(xiàn)新的安全性信號。
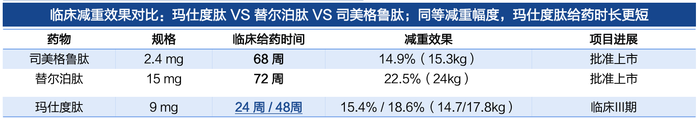
并且,2023年10月,信達(dá)生物曾公布瑪仕度肽II期臨床研究的數(shù)據(jù),治療24周后,瑪仕度肽9mg組體重較基線的平均百分比變化與安慰劑組的治療差值達(dá)?15.4%。國金證券研報曾對比瑪仕度肽與替爾泊肽、司美格魯肽的臨床減重效果顯示,同等減重幅度下,瑪仕度肽的給藥時長更短。也就是說,單從各自的臨床試驗數(shù)據(jù)來看,瑪仕度肽的減重效果較替爾泊肽、司美格魯肽更好,不過考慮到并非頭對頭臨床試驗,這一比較的參考價值有限,而瑪仕度肽頭對頭司美格魯肽的III期臨床試驗仍在進(jìn)行中。
此外,信達(dá)生物表示將在近期遞交瑪仕度肽減重適應(yīng)癥的首個新藥上市申請(NDA)。目前,國內(nèi)尚無雙靶點(diǎn)減肥藥上市。
從國內(nèi)的GLP-1減肥藥競爭格局來看,國內(nèi)華東醫(yī)藥的利拉魯肽生物類似藥和仁會生物的貝那魯肽注射液已經(jīng)獲批減重適應(yīng)癥。但是這兩款減肥藥都是GLP-1單靶點(diǎn)藥物,相較而言,瑪仕度肽的雙靶點(diǎn)激動劑效果更優(yōu)。
國內(nèi)在研的雙靶點(diǎn)減肥藥還包括博瑞生物的BGM0504、盛迪醫(yī)藥(恒瑞醫(yī)藥子公司)的HRS9531、華東醫(yī)藥的HDM1005等。不過,這幾款產(chǎn)品的研發(fā)均未到Ⅲ期。2023年7月博瑞生物的BGM0504Ⅱ期臨床獲倫理批件,盛迪醫(yī)藥的HRS9531尚處于臨床Ⅱ期,2023年12月22日華東醫(yī)藥的HDM1005臨床申請獲受理。相較而言,瑪仕度肽的進(jìn)度遙遙領(lǐng)先。
對于信達(dá)生物而言,瑪仕度肽極有可能成為繼PD-1抑制劑信迪利單抗之后的又一業(yè)績增長點(diǎn)。2023年三季度報告顯示,信達(dá)生物前三季度實(shí)現(xiàn)約41億元的總產(chǎn)品收入,而達(dá)伯舒(?信迪利單抗注射液)前三季度銷售額約為2.8億美元(約20.05億元),約占信達(dá)生物總營收的一半。
但在信迪利單抗之后,誰能撐起信達(dá)生物的業(yè)績?正處于風(fēng)口上的瑪仕度肽被寄予厚望。2023年第三季度,替爾泊肽全球銷售額達(dá)29.58億美元;2023年前三季度,司美格魯肽銷售額達(dá)142億美元。兩款減肥藥的熱賣引發(fā)了市場的無限想象,東北證券曾預(yù)測,瑪仕度肽在2025年的銷量將達(dá)到20億元。



